Эффективность применения препарата Аденопросин в комплексном лечении пациентов с хроническим бактериальным простатитом
В.Л. Медведев, М.Е. Ефремов
ГБУЗ «Научно-исследовательский институт – Краевая клиническая больница №1 им. проф. С.В. Очаповского» Министерства здравоохранения Краснодарского края, Краснодар, Россия
ФГБОУ ВО «Кубанский государственный медицинский университет» Министерства здравоохранения РФ, Краснодар, Россия
Актуальность
Хронический бактериальный простатит – распространенное заболевание, клинически диагностируемое на основании признаков воспаления и наличия инфекции в секрете предстательной железы. Стандартная антибактериальная терапия в большинстве случаев не приводит к уменьшению количества рецидивов. В связи с этим в терапии часто применяют комплексный подход и, помимо антибактериальной терапии, назначают биостимуляторы, экстракты различных растений и животных. Одним из основных преимуществ данных препаратов является минимальное количество побочных эффектов.
Цель
Оценить эффективность применения препарата АДЕНОПРОСИН® в комплексном лечении пациентов с хроническим бактериальным простатитом.
Материал и методы
Обследованы и пролечены 60 пациентов в возрасте от 24 до 50 лет (средний возраст – 31,3 ± 2,8 года) с диагнозом «хронический бактериальный простатит», продолжительность болезни составляла от 6 месяцев до 15 лет (средняя продолжительность – 1,5 ± 0,3 года). Пациенты были разделены на 2 группы: 1-я группа – 30 больных, в лечении которых на фоне антибактериальной терапии применялся АДЕНОПРОСИН®, 2-я группа – 30 пациентов, в лечении которых использовали только антибактериальный препарат. Курс лечения составил 30 дней, общее время наблюдения за пациентами – 3 месяца. Клинический контроль осуществлялся в первый визит к урологу, на 14, 28, 45 и 90-й день от начала терапии и включал заполнение пациентами опросников «Шкала симптомов хронического простатита и синдрома тазовых болей у мужчин» (National Institute of Health Chronic Prostatitis Symptom Index, NIH-CРSI), «Международный индекс симптомов при заболеваниях простаты» (International Prostate Symptom Score, IPSS) и «Шкала качества жизни» (Quality of Life, QoL), а также анкеты «Международный индекс эректильной функции» (МИЭФ-5) (International Index of Erectile Function, IIEF-5) с целью выявления возможного эффекта терапии на сексуальную функцию.
Результаты
При проведении исследования выявлено, что при применении препарата АДЕНОПРОСИН® в комплексной терапии у пациентов с хроническим бактериальным простатитом в среднем на 4 балла снижается общий балл NIH-CРSI. При проведении анкетирования по окончании лечения в 1-й группе 2 (6,6%) пациента отметили неудовлетворенность проводимой терапией, на 90-е сутки наблюдения жалобы на неудовлетворенность лечением сохранились у 1 (3,3%) больного. 5 (16,6%) пациентов 2-й группы на фоне терапии субъективно не отметили улучшения от лечения, на 90-й день наблюдения количество неудовлетворенных пациентов осталось таким же. Анализ результатов микроскопии секрета простаты и микрофлоры после лечения на 28-й день в 1-й группе показал снижение количества лейкоцитов менее 10 в поле зрения (п/з) у 25 (80%) пациентов, что выше по сравнению с пациентами 2-й группы – 21 (70%). У 5 (16,6%) пациентов 1-й группы количество лейкоцитов в секрете простаты было в интервале 10–20 в п/з, все пациенты ранее имели рецидивные формы заболевания. У 7 (23,3%) больных 2-й группы количество лейкоцитов после антибактериальной терапии – более 10 в п/з, 5 (16,6%) пациентов имели рецидивные формы заболевания, у 2 (6,6%) пациентов диагноз выявлен впервые. Это свидетельствует о том, что применение комбинированной терапии в 1-й группе в большей степени снизило воспалительные маркеры заболевания.
Выводы
Препарат АДЕНОПРОСИН® в комплексной терапии обладает доказанным противовоспалительным действием на предстательную железу, уменьшает болевой синдром, снижает общий балл простатических симптомов по NIH-CРSI, улучшает эректильную функцию, снижает маркеры воспаления в железе и может быть рекомендован пациентам с хроническим бактериальным воспалением в предстательной железе.
Ключевые слова:
хронический бактериальный простатит, АДЕНОПРОСИН®, воспаление, посев и микроскопия секрета простаты.
АКТУАЛЬНОСТЬ
Хронический бактериальный простатит – наиболее распространенное в урологической практике заболевание, клинически диагностируемое на основании признаков воспаления и наличия инфекции в секрете предстательной железы. Сопровождается клиническими симптомами (боль, нарушение мочеиспускания и сексуальной функции), длится зачастую более трех месяцев. На сегодняшний день простатит считается одной из самых распространенных патологий среди мужчин моложе 50 лет [1–4]. В отечественной урологии в амбулаторном звене на долю хронического простатита приходится примерно 20% консультаций. Это заболевание остается самой частой формой персистирующей инфекции нижних мужских мочеполовых путей [4–5].
Пусковым механизмом считается бактериальная инфекция, в большинстве своем представленная условно патогенными микроорганизмами: штаммы Enterobacteriaceae: E. coli, Klebsiella spp, E. aerogenes, различные виды Serretia, иногда неферментирующие грамотрицательные палочки: Pseudomonas aeruginosa putida [6–9].
Стандартная антибактериальная терапия в большинстве случаев не приводит к уменьшению количества рецидивов заболевания, в связи с чем часто применяют комплексный подход и также назначают биостимуляторы, экстракты различных растений и насекомых и их биологических компонентов [10]. Точный механизм действия на предстательную железу некоторых из них пока не полностью установлен и изучен. Одним из основных преимуществ данных назначений считается то, что препараты обладают минимальным количеством побочных эффектов.
В 2019 г. на фармацевтический рынок вышел новый препарат АДЕНОПРОСИН®, представляющий биомассу, полученную из личинок насекомых вида непарного шелкопряда (Lymantria dispar), которая оказывает противовоспалительное и антиоксидантное действие. Препарат представлен в виде суппозиториев. Фармакодинамика: биологически активные компоненты снижают образование фосфолипазы А2 и высвобождение арахидоновой кислоты, уменьшается проницаемость капилляров, спадает отек простаты, улучшается микроциркуляция в предстательной железе. Уже в первые дни после начала применения препарата улучшаются уродинамические параметры: увеличивается значение максимальной объемной скорости потока мочи, уменьшается время мочеиспускания, снижается количество остаточной мочи. Также отмечается улучшение общего состояние пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом, снижается индекс хронического простатита и уровень лейкоцитов в секрете простаты, улучшается однородность эхоструктуры железы. Препарат регулирует тонус и перистальтику нижних сегментов мочевыводящих путей, сокращая частоту мочеиспускания, в том числе в ночное время, а также уменьшает дизурические явления, чувство неполного опорожнения мочевого пузыря и напряжения при мочеиспускании [11].
Фармакокинетику препарата ввиду его состава в данный момент оценить не представляется возможным, в связи с чем имеется интерес в оценке эффективности лечения хронического бактериального простатита с его использованием в комбинированной терапии.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Оценить эффективность применения препарата АДЕНОПРОСИН® в комплексном лечении пациентов с хроническим бактериальным простатитом.
МАТЕРИАЛ И МЕТОДЫ
Обследованы и пролечены 60 пациентов в возрасте от 24 до 50 лет (средний возраст – 31,3 ± 2,8 года) с диагнозом «хронический бактериальный простатит», продолжительность болезни составила от 6 месяцев до 15 лет (средняя продолжительность – 1,5 ± 0,3 года).
Получено заключение этического комитета: условия проведенного исследования соответствовали общепринятым нормам морали, соблюдены требования этических и правовых норм. Проведенные исследования адекватны теме научно-исследовательской работы.
Все участники исследования были проинформированы о целях, методах, ожидаемой пользе исследования и сопряженных с участием в исследовании риске и неудобствах и дали письменное согласие на участие.
Критерии включения: пациенты с лабораторно подтвержденным диагнозом «хронический бактериальный простатит II категории (классификации простатита по NIH (Национальный институт здоровья США от 1995 г.))».
Критерии исключения: наличие острых инфекций верхних мочевых путей, острые заболевания уретры и простаты, наличие дренажей, катетеров в верхних и нижних мочевыводящих путях; заболевания, передающиеся половым путем (ЗППП); онкологические заболевания мочевыводящих путей как в анамнезе, так и подозрение на их наличие; сахарный диабет, гипогонадизм, метаболический синдром и т. д.
Все пациенты случайно разделены на две равные группы. Подтверждение воспаления в предстательной железе регистрировалось при световой микроскопии секрета простаты и определялось в случае наличия более 10 лейкоцитов в п/з. Подбор антибактериальной терапии проводился согласно культуральному исследованию секрета простаты и чувствительности микрофлоры к антибиотикам.
1-я группа – 30 пациентов, в лечении которых на фоне проводимой антибактериальной терапии применялись ректальные суппозитории АДЕНОПРОСИНА®, 2-я группа – 30 больных, в лечении которых применялся только антибактериальный препарат. Курс лечения длился 30 дней, общее время наблюдения за пациентами составило 3 месяца.
Клинический контроль осуществлялся в первый визит к урологу, на 14, 28, 45 и 90-й день от начала терапии, включал заполнение опросников «Шкала симптомов хронического простатита и синдрома тазовых болей у мужчин» (National Institute of Health Chronic Prostatitis Symptom Index, NIH-CРSI) (позволяет оценить боль: локализацию, интенсивность, частоту и продолжительность), «Международный индекс симптомов при заболеваниях простаты» (International Prostate Symptom Score, IPSS) и «Шкала качества жизни» (Quality of Life, QoL), а также анкету «Международный индекс эректильной функции» (МИЭФ-5) (International Index of Erectile Function, IIEF-5) с целью выявления возможного эффекта терапии на сексуальную функцию.
Всем пациентам при каждом визите также выполнялись пальцевое ректальное исследование предстательной железы, массаж простаты и получение секрета для микроскопического и микробиологического исследований.
Оценка результатов проводилась с помощью статистического анализа пакета прикладных программ STATISTICA 7.0, t-критерия Стьюдента для связанных выборок, t-критерия Стьюдента для несвязанных выборок. Ранжирование выборки и составление распределений частот по проведенным измерениям позволяет составить психофизиологический портрет больных мужчин с хроническим простатитом и установить существенные значения показателей диагностических измерений в проведенном исследовании. Ошибка репрезентативности распределения больных по группам – около 2,9%. Предполагаемое количество больных мужчин с урологическими заболеваниями, получающих консультацию в нашей клинике, – 20,5 тыс. чел. в год.
РЕЗУЛЬТАТЫ
При первоначальном бактериологическом исследовании секрета предстательной железы у 68% пациентов инфекция была выявлена в монофлоре (табл. 1). Исходно различий в видовом составе микрофлоры между группами установлено не было. Проверка нормальности распределения выборки «выделенная микрофлора в секрете простаты» с помощью асимметрии и эксцесса показала, что распределение выборки статистически значимо (p < 0,05) близко к нормальному распределению частот, что позволило не выделять группы антибиотиков между пациентами.
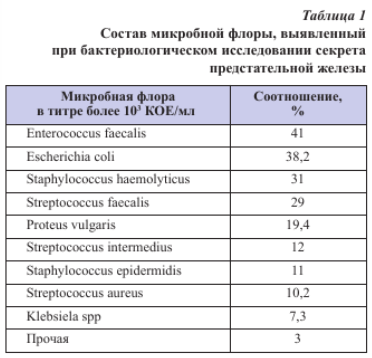
При анализе чувствительности микроорганизмов к антибактериальным препаратам получены следующие данные: 43 (72%) пациента имели чувствительность к трем и более группам антибактериальных препаратов, 10 (16%) – к двум группам антибактериальных средств и 7 (12%) – к одной группе препаратов. В качестве терапии 44 (73,4%) больным были назначены фторхинолоны (левофлоксацин принимали 29 мужчин, ципрофлоксацин – 15), 9 (15%) – цефалоспорины (цефиксим), 6 (10%) больных получали макролиды (азитромицин – 4, эритромицин – 2), одному (1,6%) пациенту были назначены аминогликозиды.
Подбор наиболее подходящего антибактериального препарата для проведения лечения согласно титру и чувствительности, возможность назначения того или иного антибиотика всегда обсуждались с клиническим фармакологом.
На момент обращения на консультацию 31 (51,7%) пациент неоднократно лечился в других клиниках по поводу диагноза «хронический бактериальный простатит», среднее число обращений составило 3,1 ± 0,6. У 29 (48,3%) больных диагноз был установлен впервые. Распределение пациентов с рецидивными формами составило равнозначное число больных, 17 пациентов вошли в первую группу и 14 – во вторую. Все мужчины, которые вошли в исследование, имели основной симптом – боль различной локализации: в промежности, в глубине таза, в наружных половых органах, проявляющуюся в виде тяжести в промежности, дискомфорта в анальном канале, жжения в уретре, не связанного с мочеиспусканием. У 24 (40%) пациентов имелись нарушения мочеиспускания при оценке анкет IPSS, которые были обусловлены не обструктивными, а ирритативными симптомами. Ирритативная симптоматика усиливалась при переохлаждении. 19 (32%) больных отметили ослабление эректильной функции, связанное с болями при эякуляции, что нами было расценено как классическая триада симптомов болезни, а не отдельное заболевание, связанное с нарушением эректильной функции. В связи с имеющимися у пациентов симптомами общее количество половых контактов в обеих группах было снижено в 1,8 раза (p ≥ 0,05).
При оценке результатов пальпации простаты у всех больных в той или иной степени были выявлены болевые ощущения. Изменения тонуса простаты при пальпации выявлены у 46 (76,6%) больных: 26 (43,3%) имели повышенный тонус, 20 (33,3%) – «пастозность».
Анализируя данные, полученные из анкет NIHCРSI, установлено, что на 14-е сутки на фоне проводимой терапии, среднее значение показателей общего балла было значимо меньше у пациентов 1-й группы (17,9 ± 2,2), в то время как у больных 2-й группы значение составило 20,2 ± 2,5 балла (p < 0,01).
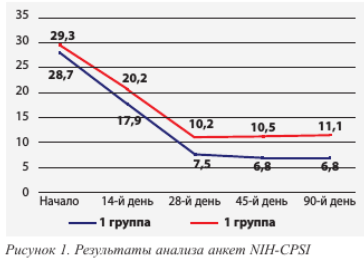
На 28-е сутки среднее значение показателей продолжало снижаться в обеих группах, сохраняя соответствующую тенденцию вплоть до 90-го дня. Динамики различия внутри групп выявлено не было.
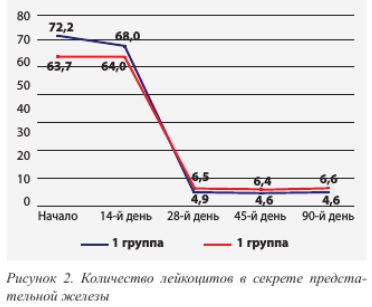
У пациентов 1-й группы количество лейкоцитов в секрете предстательной железы на 28-й день лечения составило 4,9 ± 2,7 ×109 л, а у пациентов 2-й группы – 6,5 ± 2,0 ×109 л (p < 0,01). К 90-м суткам количество лейкоцитов продолжало снижаться в обеих группах, оставаясь меньше у пациентов первой группы – 4,6 ± 2,6 ×109 л по сравнению со второй – 6,4 ± 1,3 × 109 л (p < 0,01) (рис. 2).
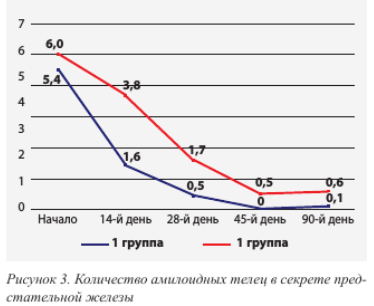
На 14-е сутки при подсчете амилоидных телец в секрете предстательной железы выявлено, что на фоне терапии среднее значение показателей меньше у пациентов 1-й группы, получавших ректальные суппозитории (1,6 ± 0,6 ед.), чем у пациентов 2-й группы (3,8 ± 1,4 ед.) (p < 0,01), с сохранением этой тенденции и на 90-е сутки в обеих группах (рис. 3).Установлено, что количество лецитиновых зерен в секрете предстательной железы на 45-й день больше у пациентов, получавших комбинированное лечение, чем у пациентов с монотерапией.
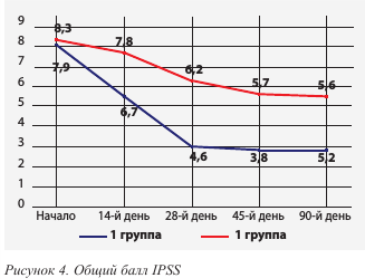
Анализ анкет IPSS выявил, что на 28-е сутки средние значения показателей в 1-й группе составили 4,6 ± 1,5 балла, во 2-й – 6,2 ± 2,4 балла (p < 0,01). На 45-е и 90-е сутки тенденция снижения баллов сохранялась, но в 1-й группе была значимо выше (рис. 4).
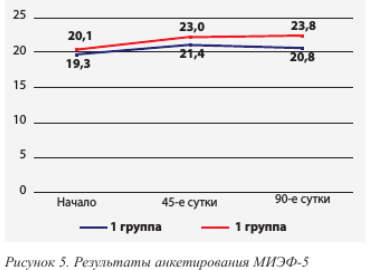
При анализе анкет МИЭФ-5 выявлено, что на 45-е сутки среднее значение показателей анкеты у пациентов 1-й группы составило 23,0 ± 2,4 балла, у пациентов 2-й группы – 21,4 ± 1,7 (p < 0,01).
На 90-е сутки показатели МИЭФ-5 повысились по сравнению с началом лечения только у пациентов 1-й группы; у пациентов, получавших только антибактериальную терапию, отмечалось незначительное повышение общего балла МИЭФ-5 (рис. 5).
ОБСУЖДЕНИЕ
Проведенный анализ выявил, что при применении препарата АДЕНОПРОСИН® в комплексной терапии у пациентов с хроническим бактериальным простатитом в среднем на 4 балла снижается общий балл анкетирования NIH-CРSI.
В свою очередь субъективно пациенты 1-й группы более удовлетворены лечением в сравнении со 2-й группой. При проведении анкетирования по окончании лечения в 1-й группе 2 (6,6%) пациента отметили неудовлетворенность от проводимой терапии, на 90-е сутки наблюдения жалобы на неудовлетворенность лечением сохранились у одного (3,3%) больного. 5 (16,6%) пациентов 2-й группы на фоне проводимой терапии субъективно не отметили улучшения от лечения, на 90-й день наблюдения количество неудовлетворенных больных осталось таким же.
Количество лейкоцитов в секрете предстательной железы на 14-е сутки у пациентов 1 группы увеличилось в среднем на 3,2 ± 0,7 в п/з, что трактовалась нами, как улучшение дренирования желез предстательной железы за счет уменьшения отека паренхимы и улучшения микроциркуляции, а также снижения застойных явлений в простате.
При анализе результатов микроскопии секрета простаты после проведенного лечения, а также микрофлоры на 28-й день у 25 (80%) пациентов 1-й группы отмечено снижение содержания лейкоцитов менее 10 в п/з, что достоверно выше по сравнению с пациентами 2-й группы – 21 (70%). У 5 (16,6%) пациентов 1-й группы количество лейкоцитов в секрете простаты было в интервале 10–20 в п/з, все пациенты ранее имели рецидивные формы заболевания. У 5 (16,6%) пациентов 1 группы количество лейкоцитов в секрете простаты было в интервале 10-20 в п/з, все пациенты ранее имели рецидивные формы заболевания. В свою очередь у 7 (23,3%) пациентов 2 группы после антибактериальной терапии, 5 (16,6%) из которых имели рецидивные формы заболевания, а у 2 (6,6%) диагноз выставлен был впервые, количество лейкоцитов в секрете простаты было более 10-20 в п/з. Это может свидетельствовать о том, что применение комбинированной терапии в 1 группе в большей степени снижает воспалительные маркеры заболевания.
Показатели анкеты IPSS продолжали снижаться у пациентов 1 группы и после окончания лечения, на 90-е сутки отмечалось снижение в среднем на один балл. Данный результат необходимо учитывать у больных с жалобами на нарушение мочеиспускания при хроническом простатите, так как это может быть связано с уменьшением объема предстательной железы на фоне снижения ее отека, а также с нивелированием ирритативной (раздражающей) симптоматики у пациентов.
При анализе анкеты МИЭФ-5 у пациентов 1 и 2 групп на 45-е сутки выявлено повышение общего балла в анкетах в среднем на 1,6 ± 0,4 балла, а на 90-е сутки сохранилось и увеличилось на 0,7 ± 0,3 балла в 1 группе и снижением общего балла на 0,6±0,2 во 2 группе. Данное наблюдение требует дальнейшего исследования. Также пациенты отмечали увеличение числа половых контактов в неделю по сравнению с периодом до лечения.
Необходимо проведение большего количества исследований с оценкой гемодинамических характеристик органов малого таза на фоне применения АДЕНОПРОСИНА®.
В результате проведенного исследования 4 пациента из 30 отметили нежелательное явление в виде разжижения кала на фоне приема суппозиториев АДЕНОПРОСИНА®, которое прекратилось после его отмены. Других нарушений, связанных с применением препарата, выявлено не было.
ВЫВОДЫ
Результаты проведенного исследования достоверно демонстрируют, что препарат АДЕНОПРОСИН® в комплексной терапии обладает доказанным противовоспалительным действием на предстательную железу; уменьшает болевой синдром, влияет на снижение общего балла простатических симптомов при анализе анкет NIH-CРSI; улучшает эректильную функцию, снижает маркеры воспаления в железе и может быть рекомендован пациентам с хроническим бактериальным воспалением в предстательной железе.
СВЕДЕНИЯ ОБ АВТОРАХ
Медведев Владимир Леонидович, д. м. н., профессор, заведующий кафедрой урологии, Кубанский государственный медицинский университет; заместитель главного врача по урологии, руководитель уронефрологического центра, Научно-исследовательский институт – Краевая клиническая больница №1 им. проф. С.В. Очаповского (Краснодар, Россия). ORCID ID: 0000-0001-8335-2578
Ефремов Михаил Евгеньевич, лаборант кафедры урологии, Кубанский государственный медицинский университет; врач-уролог, Научно-исследовательский институт – Краевая клиническая больница №1 им. проф. С.В. Очаповского (Краснодар, Россия). ОRCID ID: 0000-0003-2733-0619. E-mail: efremov.uro@yandex.ru
Финансирование
Исследование не имело спонсорской поддержки.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов
Применение препарата Аденопросин у больных хроническим абактериальным простатитом
Читать дальшеЭнтомологический препарат Аденопросин в лечении пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом
Читать дальшеАденопросин в комплексном лечении симптомов нижних мочевых путей в сочетании с простатитом III категории
Читать дальшеОценка эффективности применения энтомологического препарата «Аденопросин®» в комбинированной терапии пациентов с симптомами нижних мочевых путей, обусловленных доброкачественным увеличением предстательной железы
Читать дальшеОценка эффективности препарата Аденопросин у пациентов с хроническим простатитом
Читать дальшеЭффективность и безопасность Аденопросина при хроническом рецидивирующем бактериальном простатите с множественной устойчивостью уропатогенов, выделенных из секрета предстательной железы, к антибактериальным препаратам
Читать дальшеЭнтомотерапия – новый тренд в урологии
Читать дальшеОценка отдаленных результатов применения энтомологического препарата в комплексной терапии пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом
Читать дальшеОценка эффективности и безопасности препарата Аденопросин® у пациентов с хроническим простатитом IIIA категории
Читать дальшеСписок
литературы
2. Аляев Ю.Г., Глыбочко П.В., Пушкарь Д.Ю. (ред.) Урология. Российские клинические рекомендации. М.: ГЭОТАР-Медиа, 2018 480 с. [Alyaev YuG, Glybochko PV, Pushkar DYu (eds). Urology. Russian Clinical Guidelines. Moscow: GEOTAR-Media; 2018 480 p. (In Russ.)]
3. Rees J, Abrahams M, Doble A, Cooper A. Diagnosis and treatment of chronic bacterial prostatitis and chronic prostatitis/ chronic pelvic pain syndrome: a consensus guideline. BJU Int. 2015;116:509–25. PMID: 25711488 PMCID: PMC5008168. doi:10.1111/bju.13101
4. Аполихин О.И., Комарова В.А., Никушина А.А., Сивков А.В. Болезни предстательной железы в Российской Федерации: статистические данные 2008–2017 гг. Экспериментальная и клиническая урология. 2019;2:4–13. doi:10.29188/2222-85432019-11-2-4-12 [Apolikhin OI, Komarova VA, Nikushina AA, Sivkov AV. Prostate diseases in the Russian Federation: statistical data for 2008–2017. Experimental and Clinical Urology. 2019;2:4– 13 (In Russ.). doi:10.29188/2222-8543-2019-11-2-4-12]
5. Polackwich AS, Shoskes DA. Chronic prostatitis/ chronic pelvic pain syndrome: a review of evaluation and therapy. Prostate Cancer Prostatic Dis. 2016;19:132–8. PMID: 26951713 doi:10.1038/pcan.2016.8
6. Крупин В.Н., Белова А.Н., Крупин А.В. Лечение больных хроническим бактериальным простатитом. Вестник урологии. 2019;7(1):26–37. doi:10.21886/2308-6424-2019-7-126-37 [Krupin VN, Belova AN, Krupin AV. Treatment of patients with chronic bacterial prostatitis. Urology Herald. 2019;7(1):26– 37 (In Russ.). doi:10.21886/2308-6424-2019-7-1-26-37]
7. Kogan MI, Naboka J, Gudima I, Ibishev H. Prostatic secretion microbiota and chronic bacterial prostatitis symptoms or sings: is there a connection? Eur Urol Suppl. 2017;16(3):e145. doi:10.1016/S1569-9056(17)30152-5
8. Ibishev KS, Kogan MI, Krainiy PA, et al. Comparative analysis of clinical and laboratory parameters in patients with chronic primary bacterial prostatitis and chronic recurrent bacterial prostatitis. Eur Urol Suppl. 2019;18(2):e2330. doi:10.1016/S15699056(19)32033-0
9. Коган М.И., Набока Ю.Л., Исмаилов Р.С. Микробиота секрета простаты: сравнительный анализ хронического простатита категорий II и IIIA. Урология. 2020;2:16–22. doi:10.18565/urology.2020.2 [Kogan MI, Naboka YuL, Ismailov RS. Microbiota of prostate secretion: comparative analysis of chronic prostatitis categories II and IIIA. Urologiia = Urology. 2020;2:16–22. (In Russ.). doi:10.18565/urology.2020.2]
10. Карпов Е.И. Современный взгляд на лечение синдрома нижних мочевыводящих путей: цитомедины как класс лекарственных препаратов. Российский медицинский журнал. 2017;25(27):1992–6. [Karpov EI. Modern view on the treatment of the lower urinary tract syndrome: cytomedines as a class of drugs. Russian Medical Journal. 2017;25(27):1992–6. (In Russ.)]
11. Официальная инструкция по применению препарата аденопросин®. [Official package insert for the Adenoprosin®. (In Russ.)]
12. Dumbraveanu I, Banov P, Arian I, Tanase A. The use of entomological drugs in complex treatment of patients with chronic prostatitis and erectile dysfunction. Moldovan Journal of Health Sciences. 2017;14(4):31–43. (In Engl. and Mold.).
