Эффективность и безопасность Аденопросина при хроническом рецидивирующем бактериальном простатите с множественной устойчивостью уропатогенов, выделенных из секрета предстательной железы, к антибактериальным препаратам
Х.С.Ибишев, М.И.Коган, Ю.Л.Набока, Р.С.Исмаилов
Ростовский государственный медицинский университет, Ростов-на-Дону, Российская Федерация
Стандартная терапия хронического рецидивирующего бактериального простатита (ХРБП) антибактериальными препаратами (АБП) не всегда эффективна за счет экспоненциального роста антибиотикорезистентных штаммов уропатогенов. В связи с этим особую актуальность приобретают альтернативные подходы к лечению ХРБП.
Цель исследования: оценить эффективность применения препарата Аденопросин® в лечении пациентов с ХРБП c множественной устойчивостью уропатогенов, выделенных из секрета предстательной железы, к АБП.
Пациенты и методы. Проведено открытое одноцентровое проспективное сравнительное исследование с включением 58 пациентов с ХРБП, у которых верифицированные в секрете предстательной железы (СПЖ) уропатогены обладали множественной лекарственной устойчивостью к рекомендуемым АБП. Для оценки клинико-лабораторных показателей на всех этапах исследования (до лечения, через 1, 3, и 6 мес. после терапии) анализировались результаты анкетирования: NIH-CPSI, IPSS, лабораторных и дополнительных методов обследования. Все пациенты получали Аденопросин® в качестве монотерапии (ректально по 1 суппозиторию 1 раз в сутки), но в зависимости от длительности терапии были разделены на 2 группы: 1-я группа (n = 41) – длительность терапии составила 30 дней, 2-я группа (n = 17) – 90 дней.
Результаты. Проводимая терапия в обеих группах сопровождалась достоверным (p < 0,05) снижением выраженности симптоматики во всех периодах наблюдения согласно опросникам NIH-CPSI и IPSS и улучшением лабораторных показателей микроскопического, бактериологического и иммунологического исследований СПЖ. При общей положительной динамике большинство показателей во 2-й группе значимо (p < 0,05) отличались от таковых в 1-й группе.
Заключение. Результаты проведенного исследования достоверно демонстрируют, что препарат Аденопросин® эффективен и безопасен у пациентов с ХРБП. Аденопросин® может использоваться в качестве альтернативного метода лечения ХРБП у пациентов с множественной устойчивостью уропатогенов, выделенных из СПЖ, к АБП.
Ключевые слова: Аденопросин®, антибактериальные препараты, антибиотикорезистентность, бактерии, рецидив, простатит
Стандартная терапия хронического рецидивирующего бактериального простатита (ХРБП) антибактериальными препаратами (АБП) не всегда эффективна за счет экспоненциального роста антибиотикорезистентных штаммов уропатогенов. В связи с этим особую актуальность приобретают альтернативные подходы к лечению ХРБП [1, 2].
По мнению некоторых авторов, наличие инфекционного агента в секрете предстательной железы (СПЖ) не всегда является основным фактором развития ХРБП, так как нестерильность биологических сред, в том числе и СПЖ, – новая парадигма современной медицины [3, 4]. Для активации патогенного потенциала микроорганизмам необходим ряд предрасполагающих факторов, инициирующих инфекционно-воспалительный процесс в простате [5–7].
Одной из ведущих причин рецидива заболевания является рост резистентности микроорганизмов к АБП [8]. Данная ситуация обусловлена нерациональным и в ряде случаев неоправданным назначением антибиотиков не только пациентам с урологической патологией, но и при других нозологических формах заболеваний [9, 10]. На современном этапе изучения данной проблемы еще одним фактором, обусловливающим рост резистентности микроорганизмов к АБП, является новая коронавирусная инфекция (CОVID-19), на фоне которой в некоторых случаях необоснованно широко и длительно используются АБП различных групп для лечения бактериальных осложнений. Кроме того, SARS-CoV-2 подавляет функциональную активность различных звеньев иммунитета, что приводит к активации персистирующих и оппортунистических инфекций, в том числе и в простате [11]. Создаются благоприятные условия к появлению мультирезистентных и панрезистентных супербактерий и различных вариантов микст-инфекций, что является реальной угрозой для пациентов [10, 12]. Поэтому на сегодняшний день одна из основных задач исследователей заключается в поиске новых альтернативных антибактериальной терапии методов лечения ХРБП [13–15].
Одним из таких перспективных направлений в лечении данной патологии является применение препаратов биологического происхождения. В ряде работ было доказано, что биологические препараты обладают противовоспалительным и иммуномодулирующим эффектами, влияют на метаболические процессы в предстательной железе, усиливают синтез антигистаминовых и антисеротониновых антител и улучшают микроциркуляцию в простате, что может быть использовано в комплексной терапии ХРБП [16–18].
Среди таких препаратов в последние годы широко применяется Аденопросин®, который относится к энтомопрепаратам [18, 19]. Аденопросин® – это активное вещество, представляющее собой биомассу, полученную из личинок насекомых вида Lymantria dispar, оказывает противовоспалительное, антиоксидантное действие. Препарат снижает проницаемость капилляров, уменьшает отек простаты, улучшает микроциркуляцию в предстательной железе. Биологически активные компоненты препарата понижают образование фосфолипазы А2 и высвобождение арахидоновой кислоты со снижением синтеза простагландинов и лейкотриенов, при этом уменьшается проницаемость капилляров, чем и обусловлено снижение отека предстательной железы. На самых ранних этапах лечения эффектом Аденопросина является снижение интенсивности боли и улучшение уродинамических показателей: увеличивается значение максимальной объемной скорости потока мочи, уменьшается время мочеиспускания, снижается количество остаточной мочи, что обусловлено увеличением гемодинамических показателей простаты за счет снижения интенсивности воспаления и ишемии. На фоне приема препарата снижается уровень лейкоцитов в СПЖ, улучшается однородность эхоструктуры железы [20].
Цель исследования. Оценить эффективность применения препарата Аденопросин® в лечении пациентов с ХРБП c множественной устойчивостью уропатогенов, выделенных из секрета предстательной железы, к антибактериальным препаратам.
Материалы и методы
Дизайн исследования. Открытое одноцентровое проспективное сравнительное исследование, включающее следующие этапы: период скрининга, период лечения, период наблюдения.
Этическое одобрение. Статья одобрена локальным независимым этическим комитетом при ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России (Протокол №6/22, 24 марта 2022 г.).
Характеристика выборки.
В исследование были включены 58 пациентов с ХРБП. Всем пациентам проведено бактериологическое исследование СПЖ. В данную работу были включены только те пациенты, у которых из СПЖ выделены каузативные уропатогены в количестве >103 КОЕ/мл, но обладающие резистентностью к АБП, которые применяются для лечения ХРБП.
Критерии включения: возраст 20–45 лет, наличие симптомов ХРБП, лабораторно подтвержденный диагноз ХРБП согласно клиническим рекомендациям Минздрава России, согласие пациента участвовать в исследовании.
Критерии невключения: заболевания, передающиеся половым путем, другие заболевания простаты (гиперплазия, рак, склероз), инфекционно-воспалительные заболевания мочевых путей и репродуктивных органов, инфравезикальная обструкция мочевых путей, сопутствующие соматические заболевания, аномалии мочевых путей и репродуктивных органов, любое иммунодефицитное состояние, прием антибактериальных или других средств с антибактериальным, простатопротективным, противовоспалительным, иммуностимулирующим действием в течение 30 дней до включения в исследование.
Лабораторно-инструментальное обследование. Для оценки клинико-лабораторных показателей на всех этапах обследования анализировались результаты анкетирования по опросникам «Шкала симптомов хронического простатита и синдрома тазовых болей у мужчин» (National Institutes of Health Chronic Prostatitis Symptom Index/NIH-CРSI), «Международный индекс симптомов при заболеваниях простаты» (International Prostate Symptom Score/IPSS), а также лабораторных и дополнительных методов обследования: микроскопического, бактериологического, иммунологического исследования СПЖ, урофлоуметрии, трансректального ультразвукового исследования (ТРУЗИ). На этапе скрининга проводили комплексное клиническое обследование, направленное на оценку клинико-лабораторных показателей заболевания до лечения.
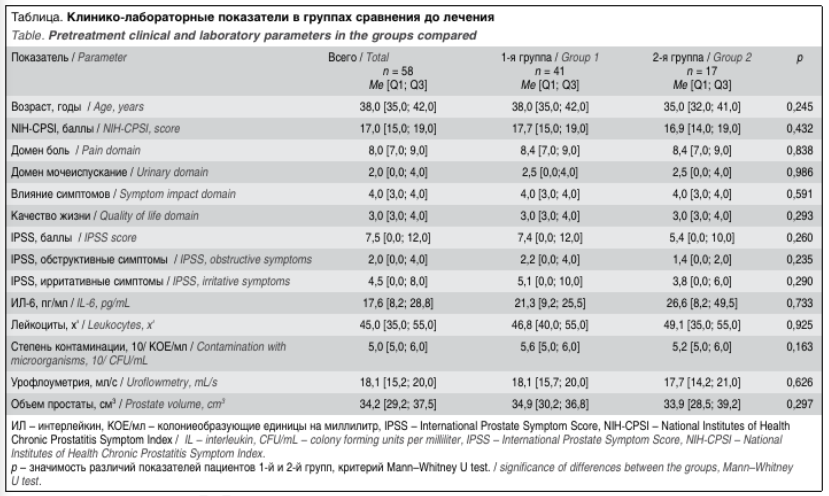
Терапия. В период лечения в качестве терапии пациенты получали Аденопросин® в виде монотерапии, согласно инструкции ректально по 1 суппозиторию 1 раз в сутки. В зависимости от длительности терапии пациенты были разделены на две группы: в 1-й группе (n = 41) длительность терапии составила 30 дней, во 2-й группе (n = 17) – 90 дней. Период наблюдения составлял 6 мес., с мониторингом клинико-лабораторных показателей, оцененных до лечения, через 1, 3, 6 мес. от начала терапии. До лечения обе группы были сопоставимы по ряду показателей (таблица).
Статистический анализ. Результаты исследования были сведены с использованием электронных таблиц Microsoft Office Excel 2010 (Microsoft Corp., США). Статистическую обработку данных проводили с использованием статистического пакета Statistica 10 (StatSoft Inc., США). Оценку соответствия распределения признаков закону нормального распределения проводили с применением критерия Shapiro–Wilk. В силу отсутствия у большинства показателей нормального распределения числовые данные представлены значением медианы (Me), первым и третьим квартилями в формате Me [Q1; Q3]. Различия числовых показателей между группами оценивали с помощью Mann–Whitney U test, значимость различий между значениями показателей на различных этапах исследования по сравнению с исходными значениями определяли с применением Wilcoxon test. Уровень значимости установлен на уровне p < 0,05.
Результаты. Проводимая терапия в обеих группах наблюдения сопровождалась статистически значимым (p < 0,05) снижением выраженности симптоматики во всех периодах исследования, согласно опросникам NIH-CPSI и IPSS, и улучшением лабораторных показателей микроскопического, бактериологического и иммунологического исследований СПЖ.
Однако при оценке результатов лечения по опроснику NIH-CPSI было выявлено, что через 1 мес. на фоне проводимой терапии в обеих группах произошло улучшение (p < 0,05) клинической симптоматики, но отмечались статистически значимые различия для некоторых показателей в группах. В частности, значение Ме для общей суммы баллов по шкале NIH-CPSI у пациентов 2-й группы было достоверно ниже (p < 0,05) через 1 мес. (7,5), а также через 3 и 6 мес. (по 2,9) по сравнению с аналогичными показателями в 1-й группе (10,2; 7,4; 7,4 соответственно) (рис. 1).
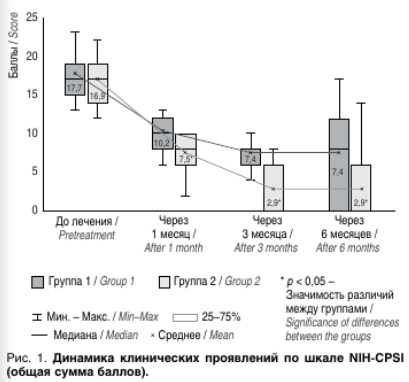
При оценке доменов боли и мочеиспускания через 1, 3, и 6 мес. наблюдения регистрировали достоверное снижение (p < 0,05) суммы баллов в обеих группах по сравнению с исходными показателями. Однако между группами были также зафиксированы значимые различия: во 2-й группе они были достоверно ниже (p < 0,05), чем в 1-й группе (рис. 2. А, В).
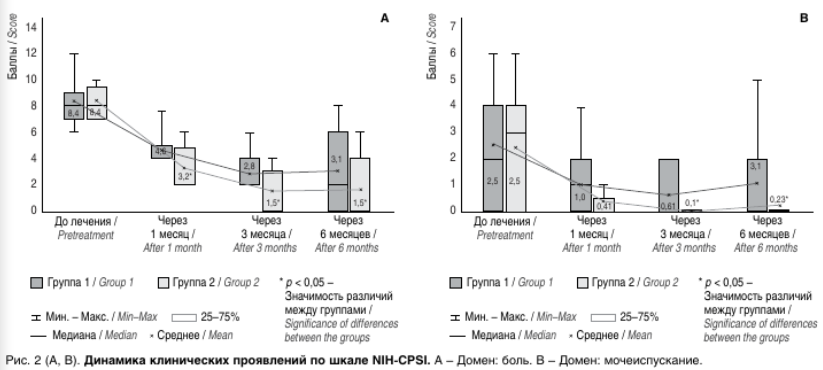
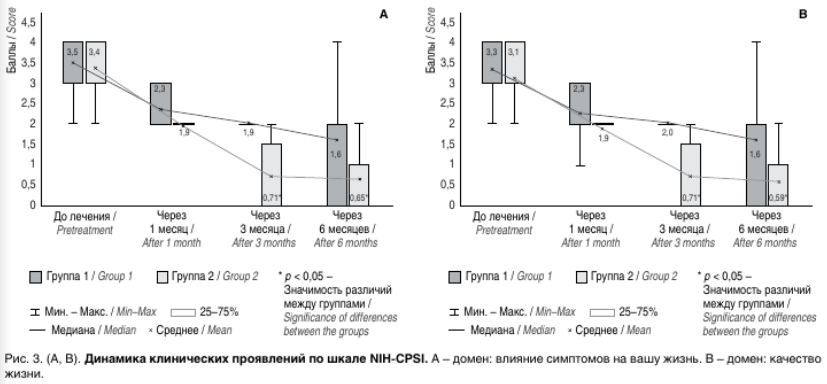
При анализе мониторинга суммы баллов доменов «влияние симптомов на вашу жизнь и качество жизни» отмечены достоверные различия между группами (p < 0,05) (рис. 3. А, В).
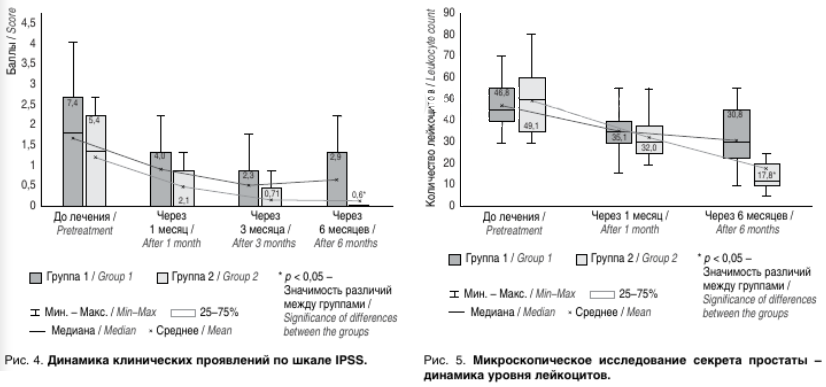
При оценке симптомов по шкале IPSS значение Ме суммы баллов до лечения в 1-й группе составляло 7,4, а во 2-й группе – 5,4. Через 1 и 3 мес. после проведенной терапии изучаемый показатель снизился в обеих группах, однако к 6-му месяцу наблюдения данный показатель в 1-й группе имел тенденцию к росту – 2,9, а во 2-й группе – к снижению до 0,6 (p < 0,05) (рис. 4).
При анализе результатов микроскопического исследования СПЖ через 1 мес. показатель Ме уровня лейкоцитов достоверно снижался (p < 0,05) в обеих группах в сравнении с исходными данными. Через 6 мес. данный показатель у пациентов 1-й группы имел незначительную тенденцию к снижению, а у пациентов 2-й группы соответствовал практически нормативным значениям (рис. 5).
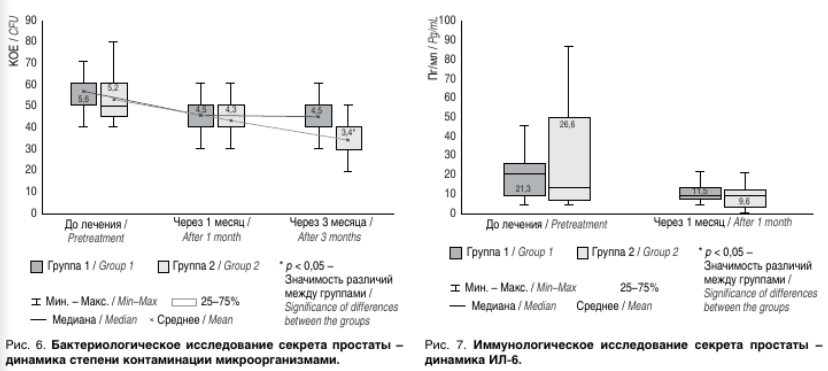
Показатель Ме степени контаминации СПЖ уропатогенами достоверно снижался (p < 0,05) через 1 мес. по сравнению с аналогичными показателями до лечения в обеих группах. Через 3 мес. регистрировали достоверное снижение обсемененности СПЖ во 2-й группе по сравнению с 1-й группой (рис. 6).
При иммунологическом исследовании СПЖ отмечено, что показатель Ме уровня интерлейкина-6 в СПЖ через 1 мес. снижался в обеих группах до нормативных значений (рис. 7).
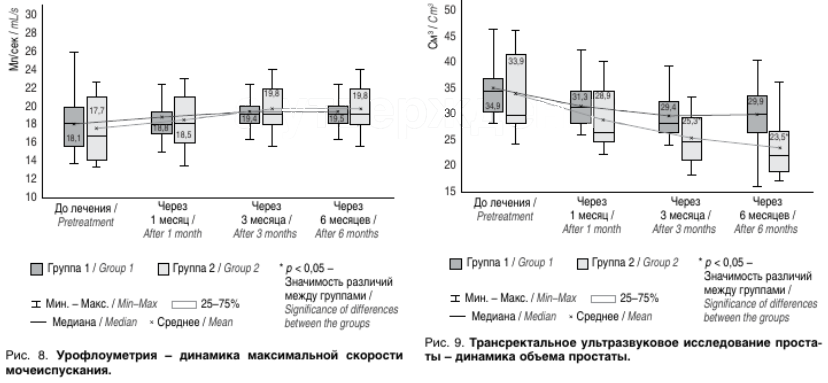
По данным урофлоуметрии на фоне проводимой терапии отмечалось улучшение максимальной скорости мочеиспускания через 1, 3 и 6 мес. наблюдения в обеих группах (p < 0,05) (рис. 8).
По данным ТРУЗИ показатель Ме объема простаты снижался во все сроки наблюдения, но с достоверными различиями (p < 0,05) через 3 и 6 мес. по сравнению с исходными результатами (рис. 9).
Обсуждение. Результаты проведенного исследования выявили, что применение препарата Аденопросин® в качестве альтернативной терапии ХРБП у пациентов с множественной устойчивостью уропатогенов, выделенных из СПЖ, к рекомендуемым АБП, приводило к улучшению как клинических, так и лабораторных показателей. Вместе с тем, согласно опроснику NIH-CPSI, субъективно пациенты 2-й группы были более удовлетворены лечением в сравнении с 1-й группой. Аденопросин® также снижает симптомы нижних мочевых путей (СНМП), согласно опроснику IPSS, что корреспондирует с ранее проведенными исследованиями [19]. Однако к полной редукции СНМП, согласно нашему исследованию, приводит лишь длительный прием Аденопросина (3 мес). При этом снижалась как ирритативная, так и обструктивная симптоматика заболевания, что определяет возможность применения Аденопросина при различном генезе СНМП и простатита (рис. 10 А, Б).
Также трехмесячный курс приема Аденопросина приводил к достоверному (p < 0,05) снижению уровня лейкоцитов до нормативных значений и степени контаминации СПЖ каузативными таксонами микроорганизмов у большинства пациентов. У пациентов 2-й группы наблюдалось достоверное (p < 0,05) снижение объема простаты в сравнении с аналогичным показателем у пациентов 1-й группы, которые получали Аденопросин® в течение 1 мес.
Полученные нами результаты могут учитываться в выборе тактики лечения пациентов с ХРБП, а также применяться для дальнейших исследований в этой области.
Заключение
Результаты проведенного исследования достоверно демонстрируют, что препарат Аденопросин® эффективен и безопасен у пациентов с ХРБП, как в группе лечения продолжительностью 1 мес., так и в группе лечения продолжительностью 3 мес.
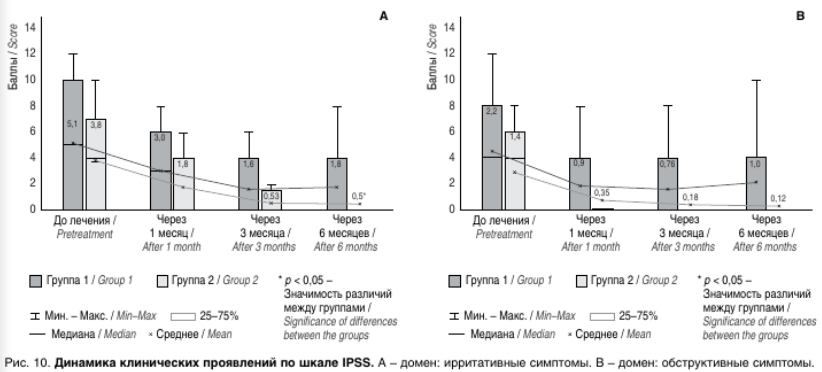
Применение Аденопросина в течение 3 мес. приводит к достоверному снижению (p < 0,05) клинических и лабораторных показателей ХРБП в сравнении с применением данного препарата в течение 1 мес.
Аденопросин® может использоваться в качестве альтернативного метода лечения ХРБП, ассоциированного с множественной устойчивостью уропатогенов, выделенных из СПЖ, к АБП.
Информация о финансировании
Финансирование данной работы не проводилось.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Информированное согласие
При проведении исследования было получено информированное согласие пациентов.
Оценка эффективности препарата Аденопросин у пациентов с хроническим простатитом
Читать дальшеОценка эффективности применения энтомологического препарата «Аденопросин®» в комбинированной терапии пациентов с симптомами нижних мочевых путей, обусловленных доброкачественным увеличением предстательной железы
Читать дальшеАденопросин в комплексном лечении симптомов нижних мочевых путей в сочетании с простатитом III категории
Читать дальшеЭнтомологический препарат Аденопросин в лечении пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом
Читать дальшеЭффективность применения препарата Аденопросин в комплексном лечении пациентов с хроническим бактериальным простатитом
Читать дальшеПрименение препарата Аденопросин у больных хроническим абактериальным простатитом
Читать дальшеЭнтомотерапия – новый тренд в урологии
Читать дальшеОценка отдаленных результатов применения энтомологического препарата в комплексной терапии пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом
Читать дальшеОценка эффективности и безопасности препарата Аденопросин® у пациентов с хроническим простатитом IIIA категории
Читать дальшеСписок
литературы
2. Винник ЮЮ, Кузьменко АВ, Гяургиев ТА. Лечение хронического простатита: современное состояние проблемы. Урология. 2021;4:138-44. DOI: 10.18565/ urology.2021.4.138-144
3. Коган МИ, Набока ЮЛ, Ибишев ХС, Гудима ИА. Нестерильность мочи здорового человека – новая парадигма в медицине. Урология. 2014;5:4852.
4. Набока ЮЛ, Коган МИ, Гудима ИА, Черницкая МЛ, Ибишев ХС, Хасигов АВ, и др. Роль неклостридиальных анаэробов в развитии инфекционно-воспалительных заболеваний органов мочевой и половой систем. Урология. 2013;6:118-21.
5. Зайцев АВ, Пушкарь ДЮ, Ходырева ЛА, Дударева АА. Хронический бактери-альный простатит, расстройства мочеиспускания у мужчин и фиброз предстательной железы. Урология. 2016;4:114-21.
6. Ибишев ХС, Крайний ПА, Манцов АА. Эффективность рекомбинантного интерферона альфа-2b в лечении хронического рецидивирующего бактериального простатита. Урология. 2020;4:21-26. DOI: 10.18565/ urology.2020.4.21-26
7. Ибишев ХС, Коган МИ, Черный АА. Клинические особенности течения хро-нического бактериального простатита на фоне дефицита тестостерона. Вестник урологии. 2013;1:39-45.
8. Котов СВ, Пульбере СА, Алесина НВ, Бояркин ВС, Гуспанов РИ, Беломытцев СВ, и др. Проблема антибиотикорезистентности микроорганизмов у пациентов с инфекциями мочевыводящих путей. Урология. 2021;1:5-12. DOI: 10.18565/urology.2021.1.5-12
9. Abushaheen MA, Muzaheed, Fatani AJ, Alosaimi M, Mansy W, George M, et al. Antimicrobial resistance, mechanisms and its clinical significance. Dis Mon. 2020 Jun;66(6):100971. DOI: 10.1016/j.disamonth.2020.100971
10. WHO Access, Watch, Reserve (AWaRe) classification of antibiotics for evaluation and monitoring of use, 2021. Geneva: World Health Organization; 2021 (WHO/ MHP/HPS/EML/2021.04). Available from: https://www.who.int/publications/i/ item/2021-aware-classification11. Ибишев ХС, Мамедов ЭА, Гусова ЗР, Паленый АИ, Прокоп ЯО. Показатели тестостерона в сыворотке крови и гемодинамики тестикул до и после инфицирования SARS-CoV-2 (пилотное исследование). Урология. 2021;5:59. DOI: 10.18565/urology.2021.5.5-9
12. Moore JE, Koulianos G, Hardy M, Misawa N, Millar BC. Antimycobacterial activity of veterinary antibiotics (Apramycin and Framycetin) against Mycobacterium abscessus: Implication for patients with cystic fibrosis. Int J Mycobacteriol. 2018 Jul-Sep;7(3):265-267. DOI: 10.4103/ijmy.ijmy_73_18
13. Magri V, Boltri M, Cai T, Colombo R, Cuzzocrea S, De Visschere P, et al. Multidisciplinary approach to prostatitis. Arch Ital Urol Androl. 2019 Jan 18;90(4):227-248. DOI: 10.4081/aiua.2018.4.227
14. Hu M, Wazir J, Ullah R, Wang W, Cui X, Tang M, et al. Phytotherapy and physical therapy in the management of chronic prostatitis-chronic pelvic pain syndrome. Int Urol Nephrol. 2019 Jul;51(7):1081-1088. DOI: 10.1007/s11255-019-02161-x
15. Кульчавеня ЕВ, Брижатюк ЕВ, Холтобин ДП, Чередниченко АГ. Современный подход к диагностике хронического простатита. Урология. 2021;2:32-39. DOI: 10.18565/urology.2021.2.32-39
16. Ибишев ХС, Манцов АА, Крайний ПА. Эффективность рекомбинантного интерферона альфа-2b в лечении хронического рецидивирующего бактериального простатита. Урология. 2020;4:21-26. DOI: 10.18565/ urology.2020.4.21-26
17. Ткачук ВН, Ткачук ИН, Боровец СЮ. Результаты 12-летнего исследования эффективности Витапроста у больных хроническим простатитом. Урологические ведомости. 2016;6(4):5-9. DOI: 10.17816/uroved645-9
18. Неймарк АИ, Неймарк БА, Борисенко ДВ, Максимова СС. Комплексная кон-сервативная терапия хронического абактериального простатита. Урологические ведомости. 2021;11(4):315-24. DOI: 10.17816/uroved71567
19. Dumbraveanu I, Ciuhrii C, Tanase A. Anti-inflamatory activity of Adenoprosin in nonbacterial prostatitis. The Moldovan Medical Journal. 2017;60(4):3-10. DOI: 10.5281/zenodo.1105101
20. Медведев ВЛ, Ефремов МЕ. Эффективность применения препарата Аденопросин® в комплексном лечении пациентов с хроническим бактериаль-ным простатитом. Инновационная медицина Кубани. 2020;3:45-51. DOI: 10.35401/2500-0268-2020-19-3-45-51
